Agrégation/Capes > Capes : montages de chimie > capes-chimie-montage-3-acides

CAPES-Montage chimie n°3 :
Expériences illustrant les propriétés des acides carboxyliques et de leur dérivés
Pour rechercher un mot dans la page, utilisez la fonction de votre navigateur
(Ctrl + F)
Introduction :
Un acide ou un dérivé d'acide est la composition : d'un groupement alkyle R plus le groupe carbonyle C=O plus un groupement Z.
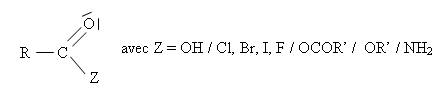
Un dérivé d'acide doit redonner l'acide carboxylique correspondant par hydrolyse.
La particularité de ces composés est la polarisation de la liaison C=O.
Les acides :
Mise en évidence de leur acidité :
Expérience :
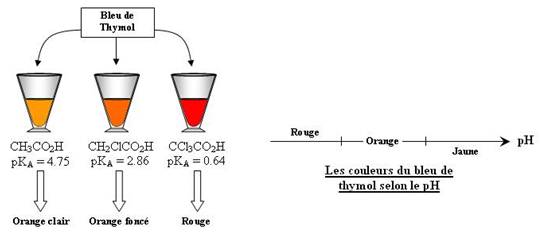
Interprétations :
Plus il y a de chlore dans le composé, plus l'acidité de celui-ci augmente.
Ceci est du à l'effet attracteur -des atomes de chlore qui l'emporte sur l'effet donneur mésomère +M.
Décarboxylation d'un acide :
Expérience :
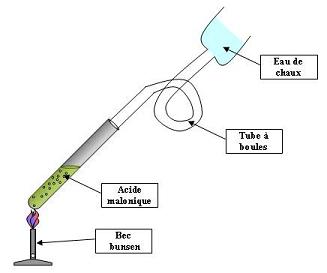
Observations :
On observe un dégagement gazeux qui trouble l'eau de chaux.
Interprétation :
Le gaz dégagé est le dioxyde de carbone CO2.
Equation de la réaction :
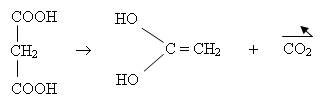
Synthèse d'un anhydride d'acide :
Expérience :
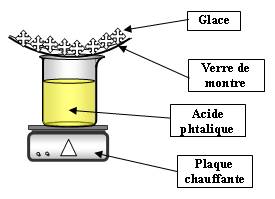
Observations :
Il y a condensation de gouttelettes sur le verre de montre, preuve de la libération de H2O.
Le produit de la réaction, lent à se former a été obtenu en préparation, on obtient un genre de toile d'araignée.
Equation de la réaction :
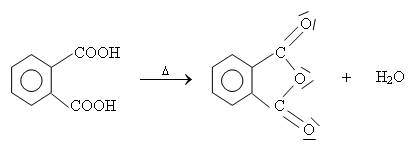
L'intérêt des anhydrides par rapport aux acides est qu'ils sont plus réactifs.
Manipulation complémentaire :
On peut mesurer le point de fusion de l'anhydride obtenu et le comparer avec le point théorique : Tfusth = 131°C.
Les dérivés d'acides :
Formation d'un polyester :
A réaliser sous hotte
Expérience :
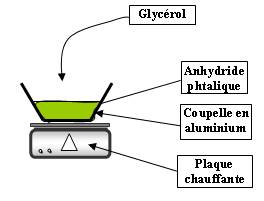
Pour procéder, il faut juste recouvrir les cristaux d'anhydride phtalique avec le glycérol (propan-1,2,3-triol).
On chauffe à couvert (en utilisant un verre de montre) 5 minutes puis à découvert pendant encore 15 minutes (il faudra donc réaliser ceci en préparation.
Observation et remarques :
La résine va durcir au refroidissement. Ce genre de résine (polyester) sont utilisées comme fibres textiles, comme solvant pour les peintures et vernis.
Synthèse d'un amide par un chlorure d'acyle :
A réaliser avec des gants et des lunettes et sous hotte
Expérience :
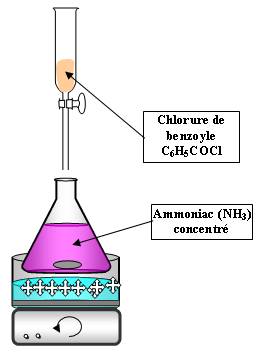
La solution est limpide au départ, lorsque l'on ajoute le chlorure de benzoyle goutte à goutte, il se forme alors un précipité blanc.
On verse ensuite le produit dans l'eau, car la réaction forme également NH4+, Cl- qui est lui aussi un précipité blanc mais soluble dans l'eau.
On récupère donc le benzamide (insoluble dans l'eau) en filtrant sur Büchner.
Manipulation complémentaire :
On mesure le point de fusion du précipité blanc au banc kofler, on trouve Tfus = 129°C (si le produit n'est pas tout à fait sec, le point de fusion mesuré aura une température plus faible ; pour éviter cela, on peut sécher le précipité à l'étuve, mais cela prend du temps).
Equation de la réaction :
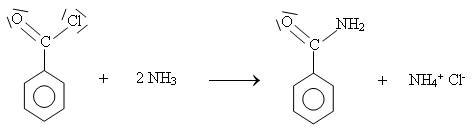
Synthèse du paracétamol par l'intermédiaire d'un anhydride d'acide :
Expérience :
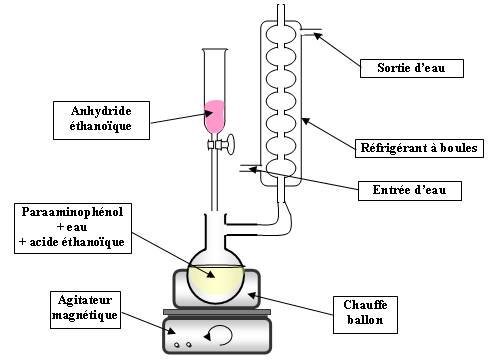
On agite le contenu du ballon 10 minutes à 80°C (ceci sera fait en préparation).
On refroidit à température ambiante puis on introduit lentement l'anhydride éthanoïque.
Après refroidissement dans la glace, le paracétamol précipite.
On récupère alors le produit par filtration Büchner.
Manipulation complémentaire :
Afin de vérifier si le produit synthétiser est bien du paracétamol, on peut prendre le point de fusion du précipité obtenu sur banc Kofler (Tfus = 168-170°C).
Equation de la réaction :
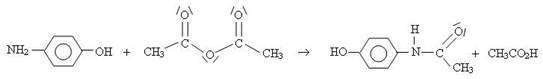
Conclusion :
Les acides et les amides sont souvent des produits naturels alors que les chlorures d'acyle et les anhydrides d'acides sont souvent fabriqués artificiellement.
Ces derniers sont importants comme intermédiaires industriels.
Remarque : différence entre polycondensation et polyaddition:
La polycondensation est une réaction entre groupements de bouts de chaîne.
Alors que la polyaddition est une réaction en chaîne : initiation, propagation, rupture.